Селективные модуляторы андрогенных рецепторов (SARM, САРМ) действуют на рецепторы андрогенов, повышая производительность и стимулируя рост мышечной массы. SARM изучаются в качестве потенциальных лекарств для терапии остеопороза, мышечной атрофии, рака и нейродегенеративных заболеваний. На SARM обращают внимания спортсмены с целью увеличения нежировой массы тела. В обзоре рассмотрен один из широко распространенных SARM – Лигандрол (Ligandrol).
Селективные модуляторы андрогенных рецепторов (SARM) были разработаны 1990-ых годах как препараты для повышения производительности, наращивания мышечной массы (анаболический эффект) и ускорения процессов восстановления, которые следуют за физическими нагрузками [1]. Наиболее перспективным направлением применения SARM считается лечение пациентов с хроническими заболеваниями, сопровождающимися истощением скелетных мышц, и замена гормона тестостерона, который долгие годы используется в терапии мышечной атрофии, но вызывает различные побочные реакции, включая маскулинизацию женщин и увеличение простаты у мужчин. Одним из эффективных SARM является Ligandrol [2].
Ligandrol, общая характеристика
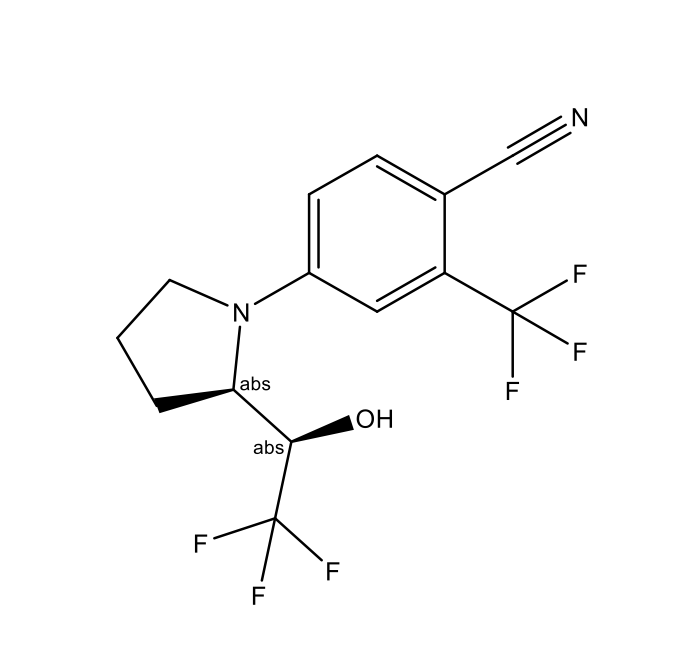
Ligandrol (VK5211, Лигандрол, LGD-4033; 4-{(2R)-2-[(1R)-2,2,2-трифтор-1-гидроксиэтил]-1-пирролидинил}-2-(трифторметил)бензонитрил; CAS 1165910-22-4) – известный представитель нестероидных SARM, обладающий хорошей биодоступностью при пероральном введении. Препарат разработан в 1999 году компанией Ligand Pharmaceuticals, занимающейся биофармацевтическими исследованиями и поиском современных подходов к терапии эндокринных заболеваний и нарушений метаболизма [3]. В 2014 году за фирмой Viking Therapeutics Inc. закреплена лицензия на Ligandrol (под шифром VK5211) с целью проведения клинических испытаний и дальнейшей разработки препарата.
В доклинических исследованиях на самках овариэктомированных крыс (т. е., с хирургически удаленными яичниками) было обнаружено, что Ligandrol способствует улучшению состояния мышечной [4]. Было проведено два эксперимента с использованием овариэктомированных крыс в качестве стандартной модели условий постменопаузы. В каждом из них трехмесячные крысы были разделены на пять групп (n = 12–15). Одна группа осталась интактной (Non-OVX), другие четыре группы были подвергнуты овариэктомии (OVX) и оставались без лечения в течение восьми (эксперимент OS) или девяти (эксперимент LG) недель. После этого крысам трех из четырех групп OVX вводили остарин или Ligandrol с дозами 0,04, 0,4 или 4 мг/кг массы тела в день в течение пяти недель. Затем крыс умерщвляли и взвешивали матку, икроножную и камбаловидную мышцы, анализировали размер волокон, плотность капилляров и активность ферментов (лактатдегидрогеназа [ЛДГ], цитратсинтаза [CS] и комплекс I). В эксперименте с применением препарата Ligandrol определяли содержание внутримышечного жира в четырехглавой мышце бедра. Все схемы введения остарина приводили к более высокой плотности капилляров в икроножных и длинных мышцах по сравнению с крысами без OVX и OVX, тогда как все варианты применения Ligandrol показали увеличенную плотность капилляров по сравнению с группой без OVX. Размер и структура мышечных волокон не изменились ни в одной из групп, получавших SARM. Активность CS была выше в длиннейшей мышце при применении остарина. Ligandrol приводил к более высокой активности CS в икроножной мышце и LDH в длиннейшей мышце. Оба SARM показали утеротрофический эффект (т. е., проявляет эстрогенные свойства), остарин в дозировке 4 и 0,4 мг, Ligandrol – 4 мг. В целом, положительный эффект на васкуляризацию мышц наблюдался для обоих SARM с более сильным влиянием в случае остарина. Ligandrol показал большее влияние на метаболизм мышц. Однако более высокий мышечный вес и содержание внутримышечного жира, наблюдаемые после применения Ligandrol в дозе 4 мг, а также утеротрофический эффект обоих SARM при высших дозировках могут рассматриваться как неблагоприятные побочные эффекты и могут быть ограничением для их применения.
Доклиническое исследование, проведенное на приматах, показало, что Ligandrol вызывает стойкое увеличение массы тела в сравнении контрольной группой и начальным уровнем по прошествии курса лечения [5]. Яванским макакам (Macaca fascicularis) вводили Ligandrol на протяжении 13 недель перорально в дозировках 0,6, 3, 15 и 75 мг/кг/день. Контрольной группе приматов назначили раствор такого же состава, но не содержащий самого препарата. После завершения курса терапии приматы показали увеличение средней массы тела на 20–47% по сравнению с исходной. Рост массы зависел от пола подопытных животных: у самцов на 29–157% больше, чем в контрольной когорте, у самок – на 100– 267% по сравнению с контролем. До 1,5 кг в среднем прибавляли массу обезьяны без учета половых различий. Важно отметить, что когорты, получавшие Ligandrol, эффективно сохраняли возросший вес, причем более 70% приобретенной массы не утрачивалось даже после четырех недель восстановительного периода по завершению эксперимента. При изученном дозировании не наблюдалось изменений в показателях электрокардиографии, частоты сердечных сокращений и по данным офтальмологического осмотра. Также не было обнаружено значительных отклонений в клинических анализах и уровнях гематологических факторов. В когортах, получавших Ligandrol, фиксировались минимальные или умеренные изменения параметров клинической патологии, которые соответствовали мощной стимуляции рецептора андрогенов.
В работе [6] было осуществлено исследование метаболизма Ligandrol и его экскреции после приема БАД, содержащей Ligandrol, определены профили выведения метаболитов и проведено сравнение времени для метаболитов фазы I и фазы II. Добавку вводили перорально единственному человеку-добровольцу и собирали образцы мочи в течение 21 дня. Анализ гидролизованных (с помощью β-глюкуронидазы), а также негидролизованных образцов был выполнен с использованием жидкостной хроматографии с масс-спектрометрией высокого разрешения в режиме отрицательной ионизации. Результаты показали, что во всех случаях два изомера дигидроксилированного метаболита являются доминирующими. Ligandrol определяется в течение 3,5 дней, его аддукт – до 6,5 дней, продукты деградации препарата – 13 дней. Глюкоконъюгированный Ligandrol и его глюкоконъюгированные метаболиты также могут рассматриваться как полезные целевые аналиты в негидролизованных образцах.
Клинические исследования Ligandrol
Было проведено клиническое испытание Ligandrol фазы I [7]. В плацебо-контролируемом исследовании 76 здоровых мужчин в возрасте 21–50 лет были рандомизированы для получения плацебо, 0,1 мг, 0,3 мг или 1,0 мг Ligandrol перорально ежедневно в течение трех недель. Препарат хорошо переносился и не показал серьезных побочных эффектов. Гемоглобин, простатспецифический антиген, аспартатаминотрансфераза (AST), ALT и интервалы QT не изменялись ни при каких примененных дозах. В дозировке 1,0 мг фолликулостимулирующий гормон и свободный тестостерон были значительно подавлены; в концентрациях лютеинизирующего гормона изменений не наблюдалось. После прекращения курса приема уровень гормонов вернулся к норме. Нежировая масса тела возрастала в зависимости от дозировки со средним приростом ~1,21 кг для 1,0 мг препарата, но статистически значимых изменений жировой или аппендикулярной массы скелетных мышц обнаружено не было. Сила, скорость подъема по лестнице и мощность имели тенденцию к дозозависимому улучшению, но не оказались статистически значимыми. Общий холестерин и липопротеины низкой плотности (ЛПНП) существенно не изменились по сравнению с исходным уровнем при любой испытанной дозе. Хотя концентрация липопротеинов высокой плотности (ЛПВП) увеличивалась при дозах 0,3 и 1,0 мг, после отмены она вернулась к норме. Уровни триглицеридов снизились по сравнению с исходным при всех дозах. Наиболее частыми побочными эффектами были головная боль и сухость во рту. Отметим, что возраст субъектов в исследовании [7] мог ограничить достоверность результатов по параметрам работоспособности, так как изученная возрастная группа вряд ли демонстрирует существенное снижение физической выносливости.
SARM рассматриваются в качестве фармакологического способа лечения мышечной атрофии. К настоящему времени завершено только одно клиническое исследование фазы II (NCT02578095), проведенное Viking Therapeutics Inc. на 108 пациентах старше 65 лет, проходящих лечение после перелома шейки бедра. Дозировки Ligandrol составляли 0,5, 1 или 2 мг. Продолжительность курса терапии составляла 12 недель. Сообщалось о дозозависимом увеличении нежировой массы тела и об увеличении проходимого расстояния за шесть минут (тест на выносливость 6MWD) на 20 метров по сравнению с плацебо [8]. К настоящему времени подробное описание результатов эксперимента не вышло в печать.
Недавно сообщали о клиническом случае, когда у здорового 24-летнего мужчины выявили симптомы гепатоцеллюлярного поражения печени [9]. Эти признаки появились через неделю после прекращения приема препарата, содержащего Ligandrol. В анамнезе отмечено, что мужчина злоупотреблял алкоголем, не использовал лекарств на постоянной основе и ранее не страдал от заболеваний печени. Вызывает беспокойство тот факт, что гепатотоксичность находится в диапазоне поражений печени, связанном с андрогенными анаболическими стероидами. Также сообщалось о 32-летнем мужчине, у которого развилось тяжелое лекарственное поражение печени после приема Ligandrol [10]. Диагноз был подтвержден биопсией, которая показала холестатический гепатит с легким портальным, перипортальным и перисинусоидальным фиброзом. Пациент рассказал, что ежедневно принимал по 1 мл раствора Ligandrol (10 мг) в течение примерно двух недель для наращивания мышечной массы (всего примерно 15 мл раствора Ligandrol). Впоследствии он почувствовал себя плохо, охарактеризовав ощущения как диффузный зуд и ломоту в теле, а затем и желтуху. Мужчина был госпитализирован на 24 часа. Пациент отрицал, что принимает какие-либо другие добавки, отпускаемые без рецепта, или прописанные лекарства. Медицинский, социальный, хирургический и семейный анамнез не внесли ясности. Симптомы включали желтуху, ахолический стул, периодические боли в животе, связанные с тошнотой, и потерю веса на 40 фунтов (18,1 кг).
Многие онлайн-блоги рекламируют Ligandrol как чрезвычайно эффективный для повышения производительности, увеличения массы, укрепления мышц и сосудов, для ускорения восстановления после нагрузок. Любителям фитнеса рекомендуют принимать от 5 до 10 мг в день курсом 6–10 недель, но предупреждают о существующем риске подавления выработки тестостерона при дозах более 10 мг. Как и родственные препараты, Ligandrol часто сочетают с другими SARM для получения усиленного эффекта. Неофициально сообщенные спортсменами нежелательные реакции были следующими: головные боли, усталость, тошнота, а также пониженное либидо, что может быть связано с подавленным уровнем тестостерона.
Следует отметить, что Ligandrol, как и другие запрещенные ВАДА вещества, был обнаружен в составе предтренировочных пищевых добавок, жиросжигателей и прогормонов [11]. По результатам анализов было показано, что в некоторых случаях препараты могут быть фальсифицированы. Тест на Ligandrol в случаях применения в качестве допинга, выявляет его в моче даже при очень низком содержании. Препарат может быть извлечен из волос в слабощелочных условиях и подвергнут LC-MS/MS анализу или LC-HRMS с предельной концентрацией до 5 пг/мг [12]. Анализ волос имеет гораздо более широкое окно обнаружения – от недель до месяцев, в зависимости от длины стержня волоса. Результаты теста волос предоставляют информацию, касающуюся длительного воздействия лекарств, хотя для некоторых препаратов было продемонстрировано, что однократное воздействие также может быть обнаружено при исследовании волос. Что касается допинговых агентов, анализ волос не признан ВАДА. Тем не менее, Спортивный арбитражный суд рассматривал несколько отчетов, в которых были представлены данные, основанные на результатах анализа волос. Отрицательный результат определения веществ по волосам не может исключить использование обнаруженного препарата и перевесить результат анализа мочи.
Заключение
При хронических заболевания, сопровождающихся мышечной атрофией, одним из путей к улучшению состояния пациентов, качества жизни и повышению их физической работоспособности является наращивание нежировой массы тела, что также ассоциируется с хорошим клиническим прогнозом [13]. Ligandrol в настоящее время не вышел из фазы испытаний, поэтому не одобрен для медицинского применения. Однако имеющиеся данные позволяют предположить, что препарат может в перспективе найти применение в терапии различных заболеваний, вызывающих атрофию мышц.
Дополнительно
САРМс (SARMs): Селективные модуляторы андрогенных рецепторов
Радарин (Radarine, RAD-140, SARM, САРМ)
Реверол, Рекардин и другие лиганды рецептора REV-ERB. При дистрофии и для регенерации мышц
Таблетки – заменители физических упражнений
No post found!
β-никотинамид-аденин-динуклеотид, НАД+
Глиптины: новый класс противодиабетических препаратов
Таблетки – заменители физических упражнений
Реверол, Рекардин и другие лиганды рецептора REV-ERB. При дистрофии и для регенерации мышц
1. Solomon, Z.J., Mirabal, J.R., Mazur, D.J., Kohn, T.P., Lipshultz, L.I., Pastuszak, A.W., Selective Androgen Receptor Modulators: Current Knowledge and Clinical Applications. Sex Med Rev, 2019. 7(1): p. 84-94. DOI: 10.1016/j.sxmr.2018.09.006.
2. The Best SARMs in 2020: Is Taking SARMs for BodyBuilding Bad for You? 2020; Available from: https://www.farrinstitute.org/best-sarms/.
3. Hamann, L.G., Mani, N.S., Davis, R.L., Wang, X.-N., Marschke, K.B., Jones, T.K., Discovery of a Potent, Orally Active, Nonsteroidal Androgen Receptor Agonist: 4-Ethyl-1,2,3,4-tetrahydro-6- (trifluoromethyl)-8-pyridono[5,6-g]- quinoline (LG121071). Journal of Medicinal Chemistry, 1999. 42(2): p. 210-212. DOI: 10.1021/jm9806648.
4. Roch, P.J., Henkies, D., Carstens, J.C., Krischek, C., Lehmann, W., Komrakova, M., Sehmisch, S., Ostarine and Ligandrol Improve Muscle Tissue in an Ovariectomized Rat Model. Front Endocrinol (Lausanne), 2020. 11: p. 556581-556581. DOI: 10.3389/fendo.2020.556581.
5. Viking Therapeutics presents new data on VK5211 demonstrating robust and durable weight gain in primates following 13 weeks of treatment. 2015; Available from: http://ir.vikingtherapeutics.com/2015-12-07-Viking-Therapeutics-Presents-New-Data-on-VK5211-Demonstrating-Robust-Weight-Gain-in-Primates-Following-13-Weeks-of-Treatment.
6. Fragkaki, A.G., Sakellariou, P., Kiousi, P., Kioukia-Fougia, N., Tsivou, M., Petrou, M., Angelis, Y., Human in vivo metabolism study of LGD-4033. Drug Testing and Analysis, 2018. 10(11-12): p. 1635-1645. DOI: https://doi.org/10.1002/dta.2512.
7. Basaria, S., Collins, L., Dillon, E.L., Orwoll, K., Storer, T.W., Miciek, R., Ulloor, J., Zhang, A., Eder, R., Zientek, H., Gordon, G., Kazmi, S., Sheffield-Moore, M., Bhasin, S., The safety, pharmacokinetics, and effects of LGD-4033, a novel nonsteroidal oral, selective androgen receptor modulator, in healthy young men. J Gerontol A Biol Sci Med Sci, 2013. 68(1): p. 87-95. DOI: 10.1093/gerona/gls078.
8. Dao, T., Green, A.E., Kim, Y.A., Bae, S.-J., Ha, K.-T., Gariani, K., Lee, M.-R., Menzies, K.J., Ryu, D., Sarcopenia and Muscle Aging: A Brief Overview. Endocrinol Metab (Seoul), 2020. 35(4): p. 716-732. DOI: 10.3803/enm.2020.405.
9. Flores, J.E., Chitturi, S., Walker, S., Drug-Induced Liver Injury by Selective Androgenic Receptor Modulators. Hepatology Communications, 2020. 4(3): p. 450-452. DOI: https://doi.org/10.1002/hep4.1456.
10. Barbara, M., Dhingra, S., Mindikoglu, A.L., Ligandrol (LGD-4033)-Induced Liver Injury. ACG Case Rep J, 2020. 7(6): p. e00370-e00370. DOI: 10.14309/crj.0000000000000370.
11. Temerdashev, A.Z., Azaryan, A.A., Labutin, A.V., Dikunets, M.A., Zvereva, I.O., Podol’skii, I.I., Berodze, G.T., Balabaev, I.A., Application of chromatography–mass spectrometry methods to the control of sport nutrition and medicines marketed via internet. Journal of Analytical Chemistry, 2017. 72(11): p. 1184-1192. DOI: 10.1134/S1061934817110090.
12. Kintz, P., Ameline, A., Gheddar, L., Raul, J.-S., LGD-4033, S-4 and MK-2866 – Testing for SARMs in hair: About 2 doping cases. Toxicologie Analytique et Clinique, 2019. 31(1): p. 56-63. DOI: https://doi.org/10.1016/j.toxac.2018.12.001.
13. Fonseca, G.W.P.D., Dworatzek, E., Ebner, N., Von Haehling, S., Selective androgen receptor modulators (SARMs) as pharmacological treatment for muscle wasting in ongoing clinical trials. Expert Opinion on Investigational Drugs, 2020. 29(8): p. 881-891. DOI: 10.1080/13543784.2020.1777275.