Ибутаморен – стимулятор секреции гормона роста, повышающий уровень инсулиноподобный фактор роста I. Экспериментальный препарат снижает содержание жировой ткани тела, положительно влияния на лиц с ожирением, улучшает метаболизм костной ткани, повышает минеральную плотность костей, помогает при катаболических состояниях и нормализует сон. Настоящий обзор раскрывает историю разработки и клинических испытаний ибутаморена.
Ибутаморен {Ibutamoren, Oratrope, Crescendo, Nutrobol, L-163,191, MK-677 (мезилат); (2-амино-2-метил-N-[1-(1-метилсульфонилспиро[2H-индол-3,4′-пиперидин]-1′-ил)-1-оксо-3-фенилметоксипропан-2-ил]пропанамид (Рис. 1); MW=528,7; CAS 159634-47-6 (свободное основание), 159752-10-0 (соль, мезилат)} представляет собой гетероциклический селективный агонист рецептора эндогенного грелина, эффективный при приеме внутрь и обладающий длительным действием; препарат стимулирует выработку гормона роста (GH) [1-4].
No post found!
Ибутаморен демонстрирует GH-рилизинг активность и повышает концентрацию в плазме крови инсулиноподобного фактора роста I (IGF-I), однако не вызывает увеличение выработки кортизола [5].
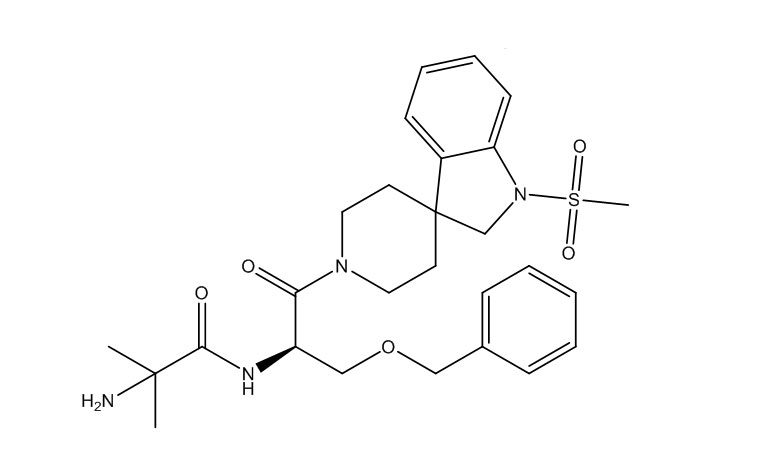
Рисунок 1 – Структурная формула ибутаморена
Ибутаморен разработан и впервые синтезирован исследователями группы лабораторий фирмы Merck & Co. (США) в 1995 году и ими же охарактеризован под шифром L-163,191 как сильный стимулятор выработки гормона роста (GH), активный при пероральном приеме, относящийся к новому, на тот момент, классу структур, действующих на активацию GH [1]. В той же работе показано, что препарат высвобождает GH из клеток гипофиза крысы в культуре с эффективной концентрацией (EC50) 1,3 нМ, причем механизм его действия практически неотличим от GH-высвобождающего пептида GHRP-6, но существенно отличается от природного соматотропин-рилизинг-гормона (GHRH). Ибутаморен повышал уровень гормона роста у собак в 4,5–5 раз относительно контрольной группы после приема внутрь в дозировке 0,125 мг/кг. Также было показано, что он специфичен к высвобождению гормона роста (увеличение до 9-кратного уровня) без значительного влияния на концентрации альдостерона, лютеинизирующего гормона, тироксина и пролактина в плазме после перорального приема 1 мг/кг, однако наблюдалось небольшое повышение уровня кортизола (в 2,4 раза). Пероральная биодоступность составляла >60%, что обусловлено его хорошей растворимостью в воде в виде кристаллической мезилатной соли, а также высокой стабильностью по отношению пептидазе, поскольку содержащиеся в нем аминокислоты, O-бензил-D-серин и α-метилаланин, представляют собой плохой субстрат для ферментативного расщепления. На основании этих свойств L-163,191 был выбран для проведения клинических исследований [1].
Старение связано со снижением активности GH, что может способствовать неблагоприятным изменениям состава тела и увеличению частоты сердечно-сосудистых заболеваний. В работе [6] было изучено стимулирующее действие ибутаморена на GH и IGF-1. В двойном слепом рандомизированном исследовании было задействовано 32 здоровых субъекта (15 женщин и 17 мужчин в возрасте 64–81 год). Они получали перорально плацебо или по 2, 10 или 25 мг препарата один раз в день в течение двух разделенных курсов по 14 и 28 дней. На исходном уровне и на 14 день каждого периода анализировали кровь для измерения уровней GH, пролактина (PRL) и кортизола. Введение ибутаморена в течение 2 недель увеличивало концентрацию GH дозозависимым образом, с увеличением среднесуточной концентрации GH при дозировке 25 мг/день на 97±23% от исходного уровня. Это увеличение было связано с усилением ранее существовавшей циклической секреции GH. Высота импульса GH и межимпульсные концентрации значительно увеличились без существенного изменения количества импульсов. При приеме ибутаморена по 25 мг/день средние сывороточные концентрации IGF-I увеличились до нормального для молодых людей диапазона (141 мкг/л на исходном уровне, 219 мкг/л через 2 недели и 265 мкг/л через 4 недели). Ибутаморен вызывал значительное повышение уровня глюкозы натощак (с 5,4 до 6,8 ммоль через 4 недели) и IGF-связывающего белка-3 (IGFBP-3). Концентрации кортизола в циркулирующей крови не изменились, а концентрации PRL увеличились на 23%, но оставались в пределах нормы [6]. Эти результаты показали перспективность применения ибутаморена в геронтотерапии.
Недельное рандомизированное двойное слепое исследование на 9 мужчинах в возрасте 27±3 лет включало пероральный приемом плацебо и дозы ибутаморена по 5 или 25 мг/день [5]. Секреции GH был близкими во всех трех группа, но частота импульсов GH возрастала с обеими дозировками препарата на ~5–10%, в первую очередь из-за увеличения количества импульсов с низкой амплитудой. Уровни IGF-I в плазме повышались дозозависимым образом, тогда как уровни IGFBP-3 были увеличены только при максимальной дозировке. Наблюдалась положительная связь между частотой пульса GH и увеличением IGF-I. За исключением некоторого повышения ночью и утром, препарат не влиял на профили кортизола. Авторы полагают, использование ибутаморена возможно для лечения относительного дефицита соматотропина [5].
Чтобы определить влияние ибутаморена, миметика GH-рилизинг-пептида (GHRP), на корреляцию GH/IGF-I у взрослых с дефицитом GH, в работе [7] изучили девять мужчин-пациентов с тяжелым дефицитом GH (пиковая концентрация гормона роста в сыворотке крови в ответ на инсулино-индуцированную гипогликемию 1,2 мкг/л, возраст 17–34 года, индекс массы тела (ИМТ) 22,6±3,3 кг/м2, которые лечились от дефицита GH в детстве с помощью GH). Субъекты получали перорально дозы 10 или 50 мг препарата один раз в сутки или плацебо в течение 4 дней в течение двух курсов лечения, разделенных по меньшей мере 28 днями. Четыре пациента получали плацебо и по 10 мг/день ибутаморена перекрестным образом в периоды 1 и 2. Пять субъектов получали по 10 мг, а затем по 50 мг/день ибутаморена с последовательно возрастающей дозой в периоды 1 и 2, соответственно. Препарат в целом хорошо переносился, без значительных изменений по сравнению с исходным уровнем циркулирующих концентраций кортизола, PRL и гормонов щитовидной железы. IGF-I в сыворотке и среднесуточные концентрации GH увеличились у всех субъектов после приема ибутаморена в дозах по 10 и 50 мг/день по сравнению с исходным уровнем. После применения 10 мг ибутаморена, концентрации IGF-I увеличились на 52±20% по сравнению с исходным уровнем, а среднесуточные концентрации GH возросли на 79±19%. После применения 50 мг ибутаморена концентрации IGF-I увеличились на 79±9%, а среднесуточные концентрации гормона роста – на 82±29%, соответственно. Концентрация IGFBP-3 в сыворотке крови возрастала как с 10 мг (с 1,2 до 1,7мкг/л), так и с 50 мг ибутаморена (с 1,7 до 2,2 мкг/л). Ответ GH на ибутаморен был выше у субъектов с исходно наименьшим дефицитом GH/IGF-I; для 10 мг ибутаморена увеличение среднесуточной концентрации GH было положительно связано как с исходной среднесуточной концентрацией GH, так и с IGF-I [7]. Инсулин натощак и после приема пищи, а также уровень глюкозы после приема пищи значительно повысились после курсов ибутаморена. Так, пероральное введение миметиков GHRP может играть роль в лечении дефицита GH в детстве.
Инверсия по действием GH отрицательного, вызванного диетой, азотистого баланса (соответствия между количеством поглощенного и выделенного организмом азота) предполагает возможную терапевтическую роль GH у пациентов с высоким катаболизмом. Двойное слепое рандомизированное плацебо-контролируемое двухпериодное перекрестное исследование [8] было направлено на изучение, может ли ибутаморен обратить индуцированный диетой катаболизм белка. Восьми здоровым добровольцам (возраст 24–39 лет) было установлено ограничение калорийности (18 ккал/кг/день) в течение двух 14-дневных периодов. В течение последних 7 дней каждого периода диеты субъекты получали перорально по 25 мг ибутаморена или плацебо один раз в день. Между циклами был установлен интервал от 14 до 21 дня. В течение первой недели ограничения калорийности суточные потери азота были одинаковыми для обеих групп (группа ибутаморена -2,67 г/день по сравнению с группой плацебо -2,83 г/день). В течение второй недели (диета и исследуемый препарат) среднесуточный баланс азота составлял 0,31±0,21 г/день в группе с ибутамореном по сравнению с -1,48±0,21 г/день в группе плацебо. Ибутаморен улучшил азотный баланс за время лечения и вызывал пиковый ответ GH 55,9±31,7 мкг/л после однократной дозы (день 1) и 22,6±9,3 мкг/л через неделю приема по сравнению с пиковыми значениями GH при использовании плацебо (примерно 9 и 7 мкг/л на 1 и 7 дни, соответственно). После начального 7-дневного ограничения калорийности уровень IGF-I снизился с 232до 186 нг/мл в группе ибутаморена и с 236 до 174 нг/мл в группе плацебо. Средняя концентрация IGF-I значительно увеличилась во время введения ибутаморена до 264 нг/мл (среднее значение за последние 5 дней лечения) по сравнению с 188 нг/мл в группе плацебо. Среднее значение IGFBP-3 за последние 5 дней применения ибутаморена также значительно увеличилось до 3273 нг/мл по сравнению с плацебо – 2604 нг/мл. Ни уровень кортизола в сыворотке, ни реакция PRL не отличались по сравнению с плацебо. Из результатов видно, что ибутаморен обращает вспять вызванное диетой азотистое истощение, и это может быть полезно при лечении катаболических состояний [8].
Двухмесячное использование ибутаморена у страдающих ожирением субъектов увеличило выработку GH, относительное повышение нежировой массы тела, а также стимулировало больший расход энергии [9]. Двойное слепое рандомизированное исследование, выполненное параллельным методом на 24 полных добровольцах (18–50 лет) с ИМТ свыше 30 кг/м2 и отношением талия/бедро более 0,95 получали лечение по 25 мг препарата или плацебо каждый день на протяжении 8 недель. По завершению, уровень IGF-I возрос примерно на 40% против плацебо. Концентрации GH, PRL и IGFBP-3 также были значительно увеличены (на ~60%), и поддерживались на повышенном уровне, кроме пикового показателя PRL, через 8 недель. Уровень кортизола в моче и сыворотке не увеличивалась относительно плацебо. Масса тела без учета жировой ткани, определенная с помощью двухэнергетической рентгеновской абсорбциометрии, существенно (на 3 кг) возросла у пациентов, принимавших ибутаморен. В целом, содержание жира практически не изменилось. Базальная скорость метаболизма значительно увеличилась через 2 недели терапии. Авторы пришли к заключению, что двухмесячное применение ибутаморена здоровыми пациентами с ожирением явилось причиной стойкого повышения концентраций GH, IGF-I и IGFBP-3 в сыворотке крови. Изменения в составе тканей организма и затратах энергии имели анаболический характер, со стабильным возрастанием количества нежировой такни и кратковременным – скорости энергетического обмена [9].
Как было показано в исследовании 1999 года [10], пероральное введение ибутаморена увеличивает маркеры метаболизма костной ткани у здоровых и функционально ослабленных пожилых людей, подобно действию гормона роста, что, вероятно, опосредуется стимуляцией циркулирующего или местного IGF-I. Авторы определили влияние хронического приема ибутаморена на сывороточный IGF-I и маркеры метаболизма костной ткани у 187 пожилых людей (65 лет и старше), включенных в три рандомизированных двойных слепых плацебо-контролируемых клинических исследования длительностью 2–9 недель. Данные «доза-ответ» были первоначально получены у здоровых пожилых людей, которые получали перорально по 10 или 25 мг ибутаморена или плацебо в течение 2 недель. Лечение 10 мг и 25 мг ибутаморена в течение 2 недель увеличивало средние уровни сшивки N-телопептида (NTX, маркер для оценки костной резорбции) в моче на 10% и 17%, соответственно, по сравнению с плацебо. Кроме того, 50 здоровых пожилых людей получали либо плацебо в течение 4 недель, либо 25 мг ибутаморена ежедневно в течение 2 недель, а затем – 50 мг ежедневно в течение 2 недель. Ибутаморен увеличивал средний уровень остеокальцина в сыворотке на 8% по сравнению с плацебо. В обоих вариантах эксперимента ибутаморен значительно повышал уровни IGF-I в сыворотке (55–94%). Впоследствии биологические эффекты ибутаморена были изучены на 105 пожилых людях, которые соответствовали объективным критериям функционального нарушения. Субъекты были рандомизированы для перорального приема доз плацебо в течение 9 недель или 5, 10 или 25 мг ибутаморена ежедневно в течение первых 2 недель с последующим приемом 25 мг ибутаморена ежедневно в течение следующих 7 недель. Лечение ибутамореном (все группы ибутаморена) в течение 9 недель увеличивало средний уровень остеокальцина в сыворотке на 29,4%, костно-специфической щелочной фосфатазы – на 10,4% и среднее выведение NTX с мочой на 22,6%. Изменение остеокальцина в сыворотке от исходного уровня коррелировало с изменением по сравнению с исходным уровнем IGF-I в сыворотке в группе ибутаморена. Авторы заключили, что ежедневное введение ибутаморена стимулирует метаболизм костной ткани у пожилых людей [10].
Те же исследователи предположили, что введение ибутаморена в комбинации с алендронатом, мощным ингибитором резорбции костной ткани, будет поддерживать более высокую скорость образования кости по сравнению с тем, что наблюдается при использовании лишь одного алендроната, тем самым вызывая большее увеличение минеральной плотности кости (МПК) у женщин с постменопаузальным остеопорозом [11]. Для этого авторы определили индивидуальные и комбинированные эффекты введения ибутаморена и алендроната или плацебо на уровни IGF-I, биохимические маркеры образования костей (остеокальцин и костно-специфическая щелочная фосфатаза) и резорбции (NTX в моче) через 12 месяцев и МПК – через 18 месяцев. В рандомизированном двойном слепом плацебо-контролируемом 18-месячном исследовании 292 женщины (64–85 лет) с низкой МПК шейки бедренной кости были случайным образом распределены в соотношении 3:3:1:1 в одну из четырех групп. Пациенты в течение 12 месяцев ежедневно получали только ибутаморен (25 мг) или алендронат (10 мг); ибутаморен (25 мг) плюс алендронат (10 мг); алендронат (10 мг); ибутаморен (25 мг); или двойное пустое плацебо. Пациенты, которые применяли только ибутаморен или плацебо в течение 12 месяцев, получали ибутаморен (25 мг) плюс алендронат (10 мг) с 12 по 18 месяцев. Все остальные пациенты продолжили назначенную ранее терапию. Все субъекты получали кальций в дозе 500 мг/сут. Первичные результаты, за исключением МПК, представлены для 12-го месяца. Ибутаморен, с алендронатом или без, увеличивал уровни IGF-I по сравнению с исходным (на 39% и 45% по сравнению с плацебо). Ибутаморен увеличивал остеокальцин и NTX в моче в среднем на 22% и 41%, соответственно (по сравнению с плацебо). Ибутаморен и алендронат снижали уменьшение костеобразования по сравнению с одним алендронатом, судя по средним относительным изменениям остеокальцина в сыворотке (-40% против -54%; комбинация против алендроната), а также влияние алендроната на резорбцию (NTX) (-52% против -61%; комбинация против алендроната). Ибутаморен плюс алендронат увеличивал МПК шейки бедренной кости (4,2% против 2,5% для алендроната). Однако аналогичного улучшения МПК поясничного отдела позвоночника, бедра в целом или костей всего тела при использовании ибутаморена плюс алендронат не наблюдалось по сравнению с одним алендронатом. GH-опосредованные побочные эффекты были отмечены в группах, получавших ибутаморен. Следует отметить, что анаболический эффект гормона роста, вызванный ибутамореном, ослаблял косвенный подавляющий эффект алендроната на формирование кости, но не приводил к значительному увеличению МПК в других местах, кроме шейки бедра. Хотя шейка бедренной кости является важным местом для предотвращения переломов, но отсутствие увеличения костной массы в частях тела по сравнению с тем, что наблюдается при использовании одного алендроната, является проблемой, если учитывать потенциальные побочными эффектами повышенной секреции GH [11].
Поскольку ранее уже было показано наличие общих механизмов, регулирующих сон и соматотропную активность, авторы работы [12] исследовали влияние длительного применения ибутаморена на качество сна у здоровых молодых и пожилых людей в двойном слепом плацебо-контролируемом трехпериодном перекрестном эксперименте. Каждый из восьми субъектов (18–30 лет) участвовал в трех 7-дневных периодах лечения с введением препарата перед сном, представленных в случайном порядке (латинский квадрат) и разделенных по меньшей мере 14 днями. Дозы ибутаморена составляли 5 и 25 мг или плацебо. Шесть пожилых субъектов в возрасте 65–71 лет аналогично участвовали в двух 14-дневных периодах лечения (с введением лекарств перед сном), разделенных 14-дневным перерывом. Дозы ибутаморена составляли 2 и 25 мг в первый и второй периоды, соответственно. Исходные данные о сне и гормональном фоне были получены за 2 дня до начала первого курса. У молодых субъектов лечение с использованием высоких доз ибутаморена привело к увеличению продолжительности стадии IV сна примерно на 50% и более чем на 20% – фазы быстрого сна по сравнению с плацебо. Частота отклонений от нормального сна снизилась с 42% при приеме плацебо до 8% при применении высоких доз ибутаморена. У пожилых людей лечение было связано с почти 50%-ным увеличением фазы быстрого сна и уменьшением латентности фазы быстрого сна. Частота отклонений от нормального сна также снизилась. Полученные данные предполагают, что ибутаморен может одновременно улучшать качество сна и корректировать относительный гипосоматотропизм при старении [12].
Так как ибутаморен все еще является экспериментальным препаратом, одобрения для использования его в медицинской практике еще не получено. Однако известно, что ибутаморен распространился в сообществе бодибилдеров. Спортсмены-любители обычно применяют данный препарат по 15 мг (до 30 мг/сутки) для набора нежировой мышечной массы. Авторами большого обзора, посвященного безопасности GH-высвобождающих препаратов, для ибутаморена рекомендуется начальная доза не более чем 25 мг перорально ежедневно, поскольку именно такая доза изучалась в рандомизированных контролируемых исследованиях [13]. Ибутаморен доступен через поставщиков в сети Интернет, поэтому при рутинном допинг-контроле с использованием общедоступных методологий, например, масс-спектрометрии, непептидные GH-высвобождающие препараты также контролируются; в моче ибутаморен обнаруживается в концентрации от 1,5•10−10 до 1,0•10−6 M [14]. Первые случаи применения ибутаморена в качестве допинга профессиональными спортсменами зафиксированы Всемирным антидопинговым агентством (ВАДА) в 2015 году [15]. Кроме того, поскольку ибутаморен химически имитирует гормон грелин, в центральной нервной системе препарат действует как нейропептид и проникает через гематоэнцефалический барьер [1-4]. Согласно недавним исследованиям, существует опасение, что он может чрезмерно стимулировать рецепторы грелина в головном мозге и приводить к нежелательному побочному действию на психику, например, усилению памяти о страхе и стресс-подобным эффектам [16].
В настоящее время доступно относительно мало исследований, изучающих эффекты GH-высвобождающих препаратов, особенно оценивающих большие когорты, хотя имеющиеся данные подтверждают их полезную роль в повышении уровня гормона роста и влиянии на результаты лечения пациентов. Очевидно, что применение ибутаморена повышает уровни GH и IGF-1, но объективных сведений о действии этих препаратов на состав тела или другие важные параметры здоровья пока недостаточно. Проведенные исследования подтверждают положительное влияние на ожирение, метаболизм костной ткани, катаболические состояния и сон, но еще предстоит изучить функциональные параметры мышц или изменения степени ожирения в контексте программы упражнений, а также данные по безопасности долгосрочного применения.
Реверол, Рекардин и другие лиганды рецептора REV-ERB. При дистрофии и для регенерации мышц
Лигандрол (Ligandrol, LGD-4033, SARM,САРМ)
САРМс (SARMs): Селективные модуляторы андрогенных рецепторов
Радарин (Radarine, RAD-140, SARM, САРМ)
Таблетки – заменители физических упражнений
1. Patchett, A.A., Nargund, R.P., Tata, J.R., Chen, M.H., Barakat, K.J., Johnston, D.B., Cheng, K., Chan, W.W., Butler, B., Hickey, G., Design and biological activities of L-163,191 (MK-0677): a potent, orally active growth hormone secretagogue. Proceedings of the National Academy of Sciences, 1995. 92(15): p. 7001. DOI: 10.1073/pnas.92.15.7001.
2. Pong, S.S., Chaung, L.Y., Dean, D.C., Nargund, R.P., Patchett, A.A., Smith, R.G., Identification of a new G-protein-linked receptor for growth hormone secretagogues. Molecular endocrinology (Baltimore, Md.), 1996. 10(1): p. 57-61. DOI: 10.1210/mend.10.1.8838145.
3. Cassoni, P., Papotti, M., Ghè, C., Catapano, F., Sapino, A., Graziani, A., Deghenghi, R., Reissmann, T., Ghigo, E., Muccioli, G., Identification, Characterization, and Biological Activity of Specific Receptors for Natural (Ghrelin) and Synthetic Growth Hormone Secretagogues and Analogs in Human Breast Carcinomas and Cell Lines1. The Journal of Clinical Endocrinology & Metabolism, 2001. 86(4): p. 1738-1745. DOI: 10.1210/jcem.86.4.7402.
4. Holst, B., Frimurer, T.M., Mokrosinski, J., Halkjaer, T., Cullberg, K.B., Underwood, C.R., Schwartz, T.W., Overlapping Binding Site for the Endogenous Agonist, Small-Molecule Agonists, and Ago-allosteric Modulators on the Ghrelin Receptor. Molecular Pharmacology, 2009. 75(1): p. 44. DOI: 10.1124/mol.108.049189.
5. Copinschi, G., Van Onderbergen, A., L’Hermite-Balériaux, M., Mendel, C.M., Caufriez, A., Leproult, R., Bolognese, J.A., De Smet, M., Thorner, M.O., Van Cauter, E., Effects of a 7-day treatment with a novel, orally active, growth hormone (GH) secretagogue, MK-677, on 24-hour GH profiles, insulin-like growth factor I, and adrenocortical function in normal young men. The Journal of Clinical Endocrinology & Metabolism, 1996. 81(8): p. 2776-2782. DOI: 10.1210/jcem.81.8.8768828.
6. Chapman, I.M., Bach, M.A., Van Cauter, E., Farmer, M., Krupa, D., Taylor, A.M., Schilling, L.M., Cole, K.Y., Skiles, E.H., Pezzoli, S.S., Hartman, M.L., Veldhuis, J.D., Gormley, G.J., Thorner, M.O., Stimulation of the growth hormone (GH)-insulin-like growth factor I axis by daily oral administration of a GH secretogogue (MK-677) in healthy elderly subjects. The Journal of Clinical Endocrinology & Metabolism, 1996. 81(12): p. 4249-4257. DOI: 10.1210/jcem.81.12.8954023.
7. Chapman, I.M., Pescovitz, O.H., Murphy, G., Treep, T., Cerchio, K.A., Krupa, D., Gertz, B., Polvino, W.J., Skiles, E.H., Pezzoli, S.S., Thorner, M.O., Oral administration of growth hormone (GH) releasing peptide-mimetic MK-677 stimulates the GH/insulin-like growth factor-I axis in selected GH-deficient adults. The Journal of Clinical Endocrinology and Metabolism, 1997. 82(10): p. 3455-3463. DOI: 10.1210/jcem.82.10.4297.
8. Murphy, M.G., Plunkett, L.M., Gertz, B.J., He, W., Wittreich, J., Polvino, W.M., Clemmons, D.R., MK-677, an Orally Active Growth Hormone Secretagogue, Reverses Diet-Induced Catabolism1. The Journal of Clinical Endocrinology & Metabolism, 1998. 83(2): p. 320-325. DOI: 10.1210/jcem.83.2.4551.
9. Svensson, J., Lönn, L., Jansson, J.O., Murphy, G., Wyss, D., Krupa, D., Cerchio, K., Polvino, W., Gertz, B., Boseaus, I., Sjöström, L., Bengtsson, B.A., Two-Month Treatment of Obese Subjects with the Oral Growth Hormone (GH) Secretagogue MK-677 Increases GH Secretion, Fat-Free Mass, and Energy Expenditure1. The Journal of Clinical Endocrinology & Metabolism, 1998. 83(2): p. 362-369. DOI: 10.1210/jcem.83.2.4539.
10. Murphy, M.G., Bach, M.A., Plotkin, D., Bolognese, J., Ng, J., Krupa, D., Cerchio, K., Gertz, B.J., Oral Administration of the Growth Hormone Secretagogue MK-677 Increases Markers of Bone Turnover in Healthy and Functionally Impaired Elderly Adults. Journal of Bone and Mineral Research, 1999. 14(7): p. 1182-1188. DOI: 10.1359/jbmr.1999.14.7.1182.
11. Murphy, M.G., Weiss, S., McClung, M., Schnitzer, T., Cerchio, K., Connor, J., Krupa, D., Gertz, B.J., Effect of Alendronate and MK-677 (a Growth Hormone Secretagogue), Individually and in Combination, on Markers of Bone Turnover and Bone Mineral Density in Postmenopausal Osteoporotic Women1. The Journal of Clinical Endocrinology & Metabolism, 2001. 86(3): p. 1116-1125. DOI: 10.1210/jcem.86.3.7294.
12. Copinschi, G., Leproult, R., Van Onderbergen, A., Caufriez, A., Cole, K.Y., Schilling, L.M., Mendel, C.M., De Lepeleire, I., Bolognese, J.A., Van Cauter, E., Prolonged oral treatment with MK-677, a novel growth hormone secretagogue, improves sleep quality in man. Neuroendocrinology, 1997. 66(4): p. 278-286. DOI: 10.1159/000127249.
13. Sigalos, J.T., Pastuszak, A.W., The Safety and Efficacy of Growth Hormone Secretagogues. Sexual medicine reviews, 2018. 6(1): p. 45-53. DOI: 10.1016/j.sxmr.2017.02.004.
14. Thevis, M., Schänzer, W., Analytical approaches for the detection of emerging therapeutics and non-approved drugs in human doping controls. Journal of Pharmaceutical and Biomedical Analysis, 2014. 101: p. 66-83. DOI: 10.1016/j.jpba.2014.05.020.
15. Mottram, D.R., Mottram, D.R., Chester, N., Drugs in sport. 7 ed. 2018: Routledge. p. 431.
16. Meyer, R.M., Burgos-Robles, A., Liu, E., Correia, S.S., Goosens, K.A., A ghrelin–growth hormone axis drives stress-induced vulnerability to enhanced fear. Molecular Psychiatry, 2014. 19(12): p. 1284-1294. DOI: 10.1038/mp.2013.135.